ことの始まり
日本人の網膜色素変性症(RP)の原因遺伝子を突き止めるべく、国立障害者リハビリテーションセンター(国リハ)の病院を訪れたRP患者68名について、既知原因遺伝子に変異がないかを検討してきました。最初に標的としたロドプシン遺伝子に、病因変異は見つかりませんでした(K07-1)。
その後、岩波氏が研究に参加し、EYS遺伝子についてスクリーニングを進めたところ、約3分の1の患者がバリアントを有しており、p.(Ser1653Lysfs)とp.(Tyr2935*)という二つが主要病因変異であることを明らかにしました(K12-1)。当時、国リハ病院には数百名のRP患者が訪れていました。そこで、さらに多くの患者の協力を得て、EYS遺伝子バリアントを明らかにすることを次の目標としました。
経緯
これまでの研究成果を踏まえて厚労科研費を2012年から3年計画で申請したところ採択されました。そこで、国リハ病院を訪れる患者の大規模リクルートを開始し、193名の協力者から血液の提供を受け、前報の68名に加え261名のゲノムDNAを得ることができました。さらに、岩波氏が京都大学医学部眼科学教室の荻野博士とコンタクトを取り、京都大病院眼科を訪れた208名のRP患者のゲノムDNAの提供を受けることになりました。両者の比較により、関東圏と関西圏の患者の変異分布の違いがわかることが期待されました。
EYS遺伝子には、エクソンの数が43個と44個の2種類のアイソフォームが報告されており、44個のアイソフォームは、余分なエクソン42を持っています。そこで本報ではエクソン42の塩基配列も決定しました。
前報でp.(Gly843Glu)が病因変異である可能性を示唆しましたが、断定するには証拠が不足していました。そこで、p.(Gly843Glu)を有する患者について、家族の方から唾液の提供を受け、家系解析を行うことにしました。また、片方のアレルにしか変異が見つからない場合、もう一方のアレルに大規模な領域の欠失や重複などの構造バリアントがある可能性を想定し、コピー数バリアント(CNV)の有無を検討することにしました。
結果
総計469名のRP患者について、エクソン42を含むEYS翻訳領域とエクソンの隣接部位の塩基配列を決定し、詳細なバリアントスペクトラムを得ることができました。前報で報告したp.(Ser1653Lysfs) (JV1) 、p.(Tyr2935*) (JV2) 、p.(Gly843Glu) (JV3)の他に、新たにp.(Gly2186Glu) (JV4)とp.(Ile2188Thr) (JV5)が複数の患者に見られ、以上5つの変異が、日本人arRP患者の主要病因変異であることが示されました(下図)。これら5つの変異を有するアレルの割合は、関東圏と関西圏で大きな差異はありませんでした。
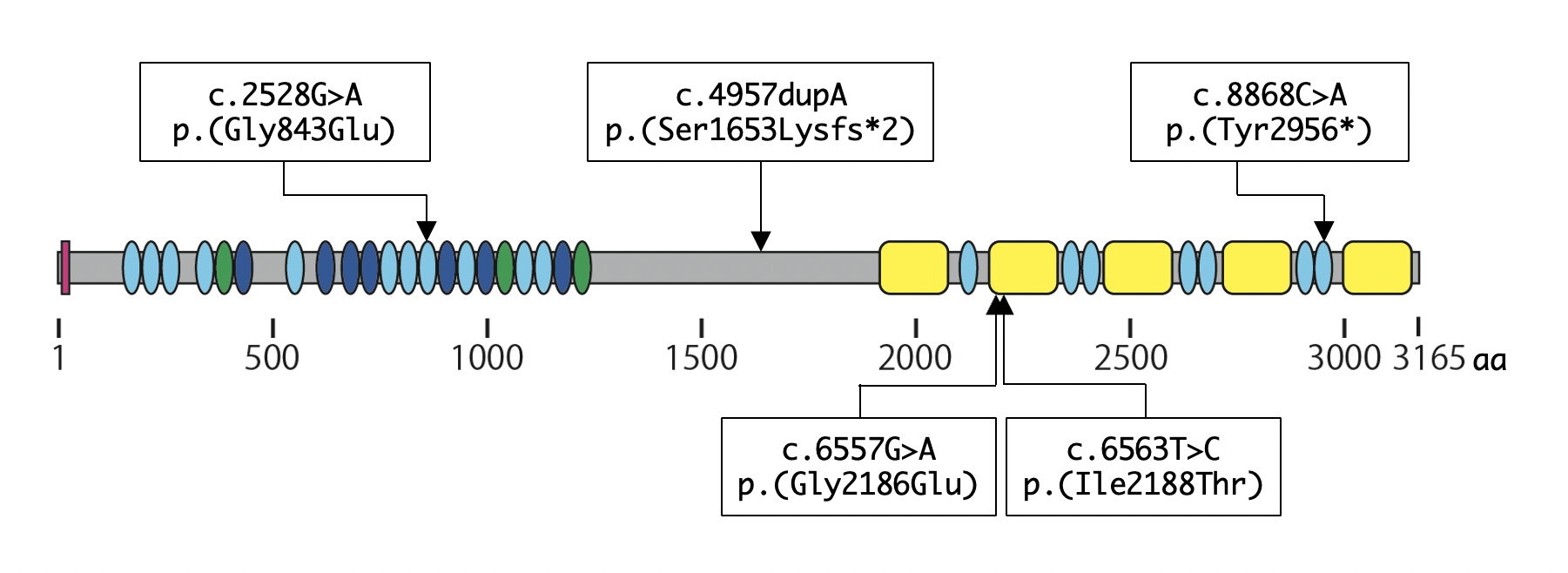
p.(Gly843Glu)は日本人集団の中にも1.9%と高頻度で見られることから、他の研究グループはこれをSNPsと考え、標的バリアントから除外してきました。しかし、我々のRP患者では6.9%と統計的に有意に差があるので、病因変異である可能性が高いと考えました。そこで、p.(Gly843Glu) (JV3) を有する10家系について分離解析(Figure 1)を行ったところ、全家系において表現型との共分離が確認でき、他の証拠と合わせて、p.(Gly843Glu)が病因変異であると結論づけました。
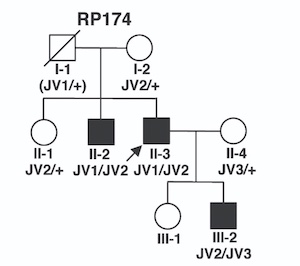
驚いたことに、5つの主要変異が組み合わさった複合ヘテロ接合を持つ患者がホモ接合のみの患者を大きく上回り、患者家系の複雑な遺伝的背景の存在が示唆されました(Table 4)。その典型的な例が、次の図に示すRP174の家系です。見かけ上、遺伝様式は常染色体優性遺伝ですが、3種の変異(JV1、JV2、JV3)が関わっています。
片方のアレルにしか変異が見つからないサンプルについて、MLPA法を用いてCNVの有無を調べたところ、7個のCNVが見出され、CNVも病因バリアントとして多く存在する可能性が示唆されました。本報は日本人RP患者のEYS遺伝子にCNVがあることを見つけた最初の論文になります。
余談
本研究は2012年から2015年にわたって実施されました。2015年までにほぼデータは出揃っていましたが、論文投稿は2019年と大幅に遅れてしまいました。2015年に、研究を主導してきた岩波氏の異動があり、また私が定年退官したためです。それでも、なんとか論文化することができ、義務を果たせました。
投稿が遅れたせいで、怪我の功名というか、論文の質を高めるというメリットもありました。Genome Aggregation Database (genomAD)やIntegrative Japanese Genome Variation Database (iJGVD)といったSNPsのデータベースが拡充し、バリアントの病原性や集団特異性の判定をするのが容易になりました。またバリアントの命名法や病原性を判定するガイドラインが新しく制定され、より精密な判定ができるようになりました。バリアントの命名法を例にとると、以前はmutationという言葉を使用していましたが、variantを使用するのが望ましいということになり、前報ではM1と呼んでいたものを、本報ではJV1と呼ぶことにしています。JVはJapanese variantの意味です。日本語では、いずれも変異と訳せますが、ここでは病因バリアントを変異と呼ぶことにしています。
疑問点
Q1 5種類の主要病因変異は、日本人特異的な変異か?
Q2 日本人集団のp.(Gly843Glu)の頻度が高いのに、RP患者にp.(Gly843Glu)ホモ接合が少ないのは何故か?
Q3 他にもCNVが存在するのではないか?
Q4 今回見出された希少バリアントの病原性は?
被引用文献
論文が出版されてからまだ日が浅いので引用数も少なく、もう少し時間が経過してからまとめる予定です。